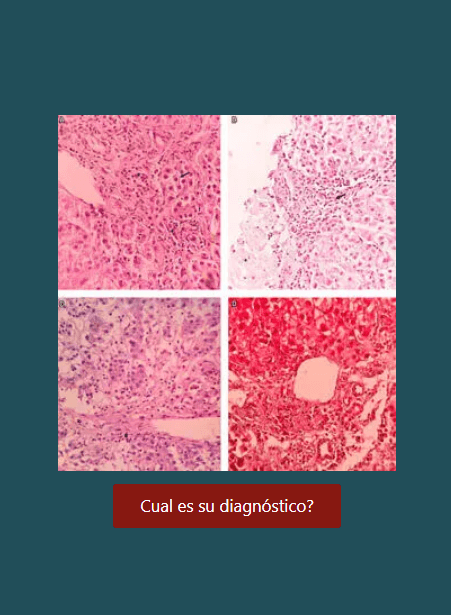
Tumor del estroma gastrointestinal (TEGI): terapia adyuvante ¿Cuánto tiempo?
DOI:
https://doi.org/10.22516/25007440.118Palabras clave:
Tumor estromal gastrointestinal, terapia adyuvante, imatinib, tratamiento, TEGI metastásico y/o avanzado, estratificación de riesgo, perfil molecular, estado mutacionalResumen
La cirugía es el tratamiento establecido para pacientes con tumor del estroma gastrointestinal (TEGI) primario completamente resecable. Luego de la cirugía, se pueden presentar recurrencias hasta en 50% de los casos en los 2 primeros años, especialmente en pacientes con alto riesgo. Esto justifica la terapia adyuvante con imatinib (IMB). Debido a la evidencia clínica, se sabe que 3 años de tratamiento es el tiempo establecido para pacientes con alto riesgo de recurrencia; sin embargo, también se conoce por los mismos estudios clínicos, que las recurrencias comienzan a detectarse de nuevo 6 a 9 meses después de suspender el medicamento.
Se presentaron 3 pacientes llevados a cirugía con resección completa de la lesión, quienes recibieron imatinib por 3 años. Meses después de suspender el medicamento, presentaron recurrencia, lo que obligó nuevamente su administración. La duración óptima del tratamiento adyuvante con IMB no está establecida, y no es claro si el IMB realmente cura la enfermedad. Por este motivo, se plantea la necesidad de revisar por cuánto tiempo se debe administrar la terapia adyuvante con IMB y el efecto que el IMB realmente tiene sobre la enfermedad. En conclusión, por la evidencia actual se sabe que la recomendación es de 3 años de tratamiento con IMB como terapia adyuvante, pero con base en la experiencia diaria y con las recomenda- ciones de expertos, existen pacientes que probablemente necesiten continuar con imatinib por mucho más tiempo mientras se informan los resultados de los estudios clínicos de 5 años de tratamiento con IMB.
Descargas
Lenguajes:
esReferencias bibliográficas
Corless C L. Gastrointestinal stromal tumors: what do we know now? Modern Pathology. 2014;27:S1-S16.
Ogata K, Mochiki E, Ojima H, et al. A Multicenter long term study of Imatinib treatment for japanese patients with unre- sectable or recurrent gastrointestinal stromal tumors. J Surg Oncol. 2014;110:942-6.
Hirota S, Isozaki K, Moriyama Y, et al. Gain of function mutation of c-KIT in human gastrointestinal stromal tumors. Science. 1998;279:577-80.
Cioffi A, Maki RG. GI stromal tumors: 15 years of lessons from a rare cancer. J Clin Oncol. 2015;33:1849-54.
Zhong JH, Ma L, Li LQ, et al. Adjuvant Imatinib for gas- trointestinal stromal tumors: the current situation and pro- blems. Scand J Of Gastroent. 2011;46:645-51.
Miettinen M, Makhlouf H, Sobin LH, et al. Gastrointestinal stromal tumors of the jejunum and ileum: a clinicopatho- logic, inmunohistochemical and molecular genetic study of 906 cases before imatinib with long term follow up. Am J Surg Pathol. Abril 2006;30(4):477-89.
Caram M, Schuetze S. Advanced or metastasic gastrointes- tinal stromal tumors: systemic treatment options. J Surg Oncol. 2011;104:888-95.
Blackstein ME, Corless CL, Ballman KV, et al. Risk assessment for tumor recurrence after surgical resection of localized primary gastrointestinal stromal tumor (GIST): North American Intergroup phase III trial ACOSOG Z9001. Presented at the 2010 Gastrointestinal Cancers Symposium: 22-24de enero de 2010; Orlando, FL, EE. UU.
Joensuu H, Eriksson M, Sundby HK, et al. One vs. three years of adjuvant imatinib for operable gastrointesti- nal stromal tumor: a randomized trial. JAMA. Marzo 2012;307(12):1265-72.
Maki R, Blay JY, Demetri G, et al. Key issues in the clinical management of gastrointestinal stromal tumors: an expert discussion. The Oncologist. 2015;20:823-30.
Reichardt P, Joensuu H, Blay JY. News fronts in the adju- vant treatment of GIST. Cancer Chemother Pharmacol. 2013;72:715-723.
Demetri G, Titton RL, Ryan DP, et al. Case 32-2004: a 68 year old man with a large retroperitoneal mass. N Engl J Med. 2004;351(17)21:1779-87.
Blay JY, Casali PG, Dei Tos AP, et al. Management of gas- trointestinal stromal tumour: current practices and visions for the future. Oncology. 2015;89:1-13.
Demetri G, Mehren M, Antonescu C, et al. NCCN Task Force Report: update on the management of patients with gastrointestinal stromal tumors. J Natl Compr Canc Netw. 2010;8(2):S1-41.
ESMO. European Sarcoma Network Working Group: Gastrointestinal stromal tumors. ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2012;23(l7):vii49-55.
Bischof DA, Dodson R, Jimenez MC, et al. Adherence to guideliness for adjuvant imatinib therapy for GIST: a multi- institutional analysis. J Gastrointest Surg. 2015;19:1022-8.
Sicklick JK, Lopez N. Optimizing surgical and imatinib the- rapy for the treatment of gastrointestinal stromal tumors. J Gastroint Surg. 2013;17:1997-2006.
Miettinen M Lasota J. Gastrointestinal stromal tumors: pathology and prognosis at different sites. Semin Diagn Pathol. 2006;23(2):70-83.
Telzlaff E, Davey M. Optimizing adherence to adjuvant Imatinib in gastrointestinal stromal tumor. J Adv Pract Oncol. 2013;4(4):238-50.
Gold JS, Gonen M, Gutierrez A, et al. Development and validation of a prognostic nomogram for recurrence free survival after complete surgical resection of localized pri- mary gastrointestinal stromal tumor: a retrospective analy- sis. Lancet Oncol. 2009;10(11):1045-52.
Rossi S, Miceli R, Messerini L, et al. Natural history of ima- tinib naive GISTs: a retrospective analysis of 929 cases with long term follow and development of a survival nomogram base don mitotic index and size as continuous variables. Am J Surg Pathol. 2011;35:1646-56.
Pracucho EM, Lopes LR, Zanatto RM, et al. Profile of patients with gastrointestinal stromal tumors. Arq Bras Cir Dig. 2015;28(2):124-7.
Trent JC, Subramanian MP. Managing GIST in the Imatinib era: optimization of adjuvant therapy. Expert Rev Anticancer Ther. 2014;14(12):1445-59.
Dematteo RP, Ballman KV, Antonescu CR, et al. Long term results of adjuvant imatinib mesylate in localized high-risk primary gastrointestinal stromal tumor. ACOSOG Z9000 Intergroup phase 2 Trial. Ann Surg. 2013;258(3):422-9.
Dematteo RP, Ballman KV, Antonescu CR, et al. Adjuvant Imatinib mesylate after resection of localized primary gas- trointestinal stromal tumours: a randomized, double-blind placebo controlled trial. Lancet. 2009:373(9669):1097-104.
Niazi AK, Kaley K, Saif W. Gastrointestinal stromal tumor of colon: a case report and review of literature. Anticancer Research. 2014;34:2547-50.
Le Cesne A, Coquard IR, Bui BN, et al. Discontinuation of Imatinib in patients with advanced gastrointestinal stromal tumors after 3 years of treatment: an open label multicenter randomized phase 3 trial. Lancet Oncol. 2010;11:942-9.
Novartis Pharmaceuticals. Five year adjuvant Imatinib mes- ylate (Gleevec) in gastrointestinal stromal tumor (GIST). 2012. Disponible en: http//clinicaltrials.gov/ct2/show/ NCT00867113
Ray Coquard IL, Bin Bui N, Adenis A, et al. Risk of relapse with Imatininb (IM) discontinuation at 5 years in advanced GIST patients: results of the prospective BFR14 randomi- zed phase III study comparing interruption versus continua- tion of IM at 5 years of treatment: a French Sarcoma Group Study. J Clin Oncol (Meeting Abstracts). 2010;28:10032.
Knox P. Adjuvant Imatinib study updates results. 15 de diciembre de 2015. Disponible en: https://liferaftgroup. org/2015/12/adjuvant-imatinib-study-updates-results/
Le Cesne A, Blay J Y, Reichardt P, et al. Optimizing tyrosine kinase inhibitor therapy in gastrointestinal stromal tumors:
exploring the benefits of continuous kinase suppression.
The Oncolgyst. 2013;18:1192-9.
Reichardt P, Blay JY, Boukovinas I, et al. Adjuvant therapy in
primary GIST: state of the art. Ann of Oncol. 2012;23:2776-81.
Joensuu H, Roberts PJ, Sarlomo Rikala M, et al. Effect of the tyrosine kinase inhibitor ST1571 in a patient with a metastasic gastrointestinal stromal tumor. N Engl J Med. 2001;344:1052-6.
Joenssu H, Hohenberger P, Corless CH. Gastrointestinal stromal tumor. Lancet. 2013;382:973-83.
Heinrich MC. Imatinib treatment of metastasic GIST: don’t
stop (believing). Lancet Oncol. 2010;11:910-1.
Bauer S, Fletcher J. El descubrimiento de nuevas terapias es posible si comprendemos como se desarrolla un GIST. Disponible en: http://alianzagist.org/assets/nuevas-terapias.pdf
Balachandran VP, DeMatteo RP. Targeted therapy for cancer. The Gastrointestinal Stromal Tumor Model. Surg Oncol Clin N Am. 2013;22:805-21.
Balachandran VP, DeMatteo RP. Gastrointestinal stro-
mal tumors. Who should get imatinib and for how long? Advances in Surgery. 2014;48:165-83.
Descargas
Publicado
Cómo citar
Número
Sección
Licencia
Aquellos autores/as que tengan publicaciones con esta revista, aceptan los términos siguientes:
Los autores/as ceden sus derechos de autor y garantizarán a la revista el derecho de primera publicación de su obra, el cuál estará simultáneamente sujeto a la Licencia de reconocimiento de Creative Commons que permite a terceros compartir la obra siempre que se indique su autor y su primera publicación en esta revista.
Los contenidos están protegidos bajo una licencia de Creative Commons Reconocimiento-NoComercial-SinObraDerivada 4.0 Internacional.


| Estadísticas de artículo | |
|---|---|
| Vistas de resúmenes | |
| Vistas de PDF | |
| Descargas de PDF | |
| Vistas de HTML | |
| Otras vistas | |